一、“一滴血”实现肿瘤精准检测
——基于cfDNA多组学的癌症早筛早诊关键技术

癌症早诊早治是癌症诊治的关键,早期癌症的5年生存率可以达到80~90%,而晚期癌症的5年生存率只有不到30%。利用液体活检多组学(甲基化、CNV及突变等)技术,获取血液中游离的DNA(cfDNA)信息,有助于避免肿瘤异质性问题,能够全面分析肿瘤突变情况,为肿瘤早期诊断提供供更多的决策依据。
谷红仓研究员团队在DNA甲基化技术开发、泛癌种多组学液体活检早筛早诊技术开发及临床转化等方面取得重要进展。研究成果发表在《Nature》、《Cell》等全球顶级期刊。
该原创性技术的临床转化将推动肿瘤的早筛和早诊,降低肿瘤对全民健康的危害和医疗负担。

1. 核心技术:研发甲基化原创测序技术
在国际上最先把高通量技术引入表观遗传学研究,开发了六项原创技术,包括:最先在国际上将高通量测序技术与DNA甲基化研究结合报道了简化DNA甲基测序技术(RRBS);最早在国际上将DNA甲基化和组蛋白修饰测序技术结合报道了免疫共沉淀甲基化测序技术(CHIP-BS-Seq)。
2. 技术应用:基于多组学液体活检技术的癌症筛查
研究团队率先利用cfDNA-RRBS技术,构建肿瘤预测模型,预测患癌风险。预测模型灵敏度为87.9%,已达到国外领先水平。
3. 技术应用:基于血液cfDNA甲基化的肺结节良恶性无创诊断
研究团队利用一种新型的血液游离DNA(cfDNA)全基因组甲基化测序技术(cfMeDIP-seq)发现了肺癌病人与健康人cfDNA差异的甲基化特征区域,并且通过人工智能的方法建立了肺结节良恶性诊断模型。该模型区分肺癌的敏感性和特异性分别达到91.0%和93.3%。
二、“一口气”完成肿瘤快速筛查
——呼气质谱肿瘤快速无创筛查技术与装备

“闻诊”新突破, “嗅”出癌细胞。呼气看似无形,其实每一口呼出的气都包含着反映身体各器官生理/病理状态的生物信号分子——挥发性有机物(volatile organic compound,VOC)。基于VOCs的呼气检测进行疾病筛查和辅助诊断,因为安全无创、简捷便利、检查费用低、接受度高等优点,正成为疾病无创诊断的重要发展方向。
储焰南研究员团队通过近十年的努力,突破并掌握了超高灵敏关键技术,自主研制出了国内第一台呼气质谱检测仪,只需7秒就能完成对一名受试人员呼气的直接测量,通过分析呼出气体中标志性的挥发有机物VOC,研究VOC的种类、浓度与肿瘤的关联性,建立癌症早期诊断和无创筛查新方法,目前在食管癌、肺癌、宫颈癌等类型肿瘤的实验判别准确率达到90%。目前,团队承担相关国家重点研发计划、国家自然科学基金等项目40余项。
该专利仪器有望为肿瘤的早期筛查与辅助诊断提供一种高通量无创检测技术新方法。

1. 核心技术:自主研制呼气质谱检测仪
研究团队历经10余年,突破高灵敏关键技术,研制呼气检测质谱仪,并建设了VOC气体活检研究平台,开展了人体、动物、细胞科学实验,研究了人体呼气与细胞培养条件下影响肿瘤标志物的因素,初步建立食管癌、宫颈癌等恶性肿瘤无创筛查新方法。
2. 研究发现:食管癌患者呼气特征的PTR-MS检测
研究团队利用自主研发的实时在线检测呼气质谱仪,只需7秒就能完成对一名受试人员呼气的直接测量。研究发现区分食管癌的七种呼气质谱特征离子,用于甄别是否患食管癌的真阳性率和真阴性率分别达到86.2%和89.5%。
3. 研究发现:宫颈癌患者呼气特征的PTR-MS检测
通过对13名宫颈癌患者和34名健康人的呼气检测,统计发现区分宫颈癌的四种呼气质谱特征离子,用于判别宫颈癌的真阳性率和真阴性率分别达到92.3%和88.2%。
三、“药物敏感”助力肿瘤精准选药
——HDS肿瘤高通量药敏检测技术
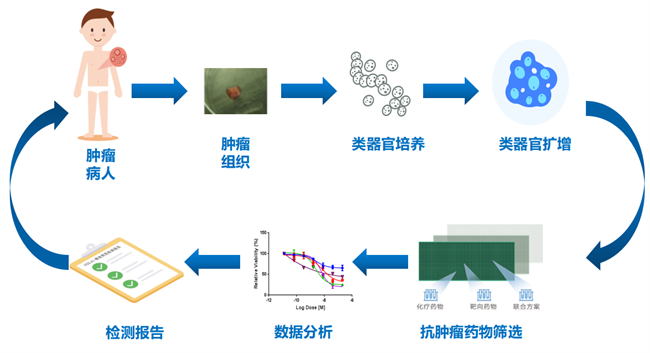
HDS肿瘤高通量药敏检测技术(High-throughput Drug Sensitivity analysis Strategy)是基于细胞水平在体外检测药物敏感性的一种技术,即将患者肿瘤细胞与待测药物直接相互作用,通过观察药物对细胞活力的影响,分析患者细胞对待测药物的敏感性,为没有靶向药物可用或者靶向药物无效的肿瘤患者提供个性化的精准选药指导。
刘青松研究员团队首创的针对肿瘤患者的精准用药技术体系,突破了传统药敏试验细胞分离培养难的核心技术问题,利用改进后CRC(Conditionnally Reprogrammde Cell)技术实现了在短期内大量扩增富集,保持患者体内癌细胞基因特性和药敏特性的原代癌细胞(培养出“试管里的病人”),能够在短期内为肿瘤患者提供全面的用药检测,从3000余种药物中进行科学精准选药。团队目前已申请相关专利技术30余项,覆盖十余个癌种,服务患者20000余人。
该技术的运用,解决了肿瘤患者早期精准选药、晚期无药可吃的问题,避免无效治疗和以人试药,显著提升了患者用药有效率。

1. 核心技术:原代细胞可再生技术
近年来,针对食管癌、肺癌、胃癌等十余种常见肿瘤,开发出可体外快速高保真扩增的培养方法,包括2D体系和3D类器官体系,申请专利30余项。体外扩增后的原代细胞在基因和病理方面保持了初始临床样本的特征,整体培养成功率超过80%。
2. 技术应用:解决早期/初诊肿瘤患者精准选药问题,解决晚期/复发/耐药的肿瘤患者无药可吃问题
HDS技术的运用,对于早期/初诊的肿瘤患者,解决了指南内多选药物的精准使用问题,避免无效治疗、过度治疗和以人试药;对于晚期/复发/耐药的肿瘤患者,HDS技术解决了他们无药可吃的问题,让患者“有药可吃,吃有效药”,提高患者带瘤生存质量,延长生命周期。
四、“药物浓度”指导肿瘤精准用药
——基于SERS技术的药物浓度监测新方法
表面增强拉曼光谱,简称SERS,是指当分子吸附在粗糙贵金属表面或纳米表面上,通过一定增强原理使其拉曼散射信号强度成指数倍数增长的一种光谱现象。作为一种新兴的检测方法,SERS技术具有极高的检测灵敏度、可提供丰富的物质结构信息并具有无损检测的特点。基于SERS技术的药物浓度监测,可以精准分析测定药物在不同患者血液中的浓度,用以评价疗效或确定给药方案,使给药方案个体化。
杨良保研究员团队通过建立并发展拉曼光谱分析的原理和方法体系,开展表面增强拉曼光谱技术在重大疾病检测领域研究,研发抗肿瘤药物浓度动态监测方法与仪器,以达到“量体裁衣”的肿瘤患者个性化用药方案。目前,团队承担相关国家重大科学仪器设备开发专项、国家重大新药创制专项、国家自然科学基金等项目20余项,相关研究成果获得国家技术发明二等奖1项和安徽省自然科学奖一等奖1项。
该技术的研发应用,有利于提高疗效,降低过度用药产生的不良反应,指导个体化药物治疗方案的设计与实施。

1. 研究发现:药物浓度分析方法和仪器研制
研究团队开展新型分离介质研究和新型样品前处理技术、装置、分析方法研究,合成新型大面积高重复性贵金属纳米阵列增强芯片,构建高灵敏与高稳定信号强度输出体系,发展各种药物浓度SERS检测方法,开发基于SERS的血药浓度检测设备。设计并制作出可个性化检测-分析-给药的临床药物治疗系统装置。
2. 研究发现:手持拉曼光谱仪快速监测和定量检测抗肿瘤药物氟尿嘧啶
研究团队利用液体三相平衡原理控制液滴的收缩,不仅形成高密度、高稳定的液态3D热点矩阵,而且使抗肿瘤药物能够自主进入热点区域。结合自主研发的手持式拉曼光谱仪,能够实现对肿瘤病人血清中抗癌药物氟尿嘧啶的在线定量检测。
五、“等离子体”提供肿瘤治疗新手段
——大气压低温等离子体无创肿瘤治疗新技术

等离子体是继固态、液态、气态之后的物质第四态,当外加电压达到击穿电压时,气体分子被电离,产生包括电子、离子、原子和原子团在内的混合体。大气压低温等离子体具有选择性杀死肿瘤细胞、适应肿瘤种类多的优势,是癌症治疗的新方法。
韩伟研究员团队探索这种革命性的全新抗癌疗法,发现低温等离子体可以有效抑制或杀伤肺癌、宫颈癌、鼻咽癌、皮肤癌等肿瘤细胞,明确了等离子体对癌细胞的作用规律和生物学效应,以期对现有肿瘤治疗方法进行有益补充。该项研究得到了时任国务院副总理刘延东的重要批示,指示我院进一步加快研究成果的临床转化,为癌症治疗提供—种全新的手段和方法。目前,团队承担相关国家自然基金重点项目、国家基金委重大科研仪器设备研制专项、中国科学院“百人计划”等项目10余项。
等离子治癌目前在国际上还没有成熟的临床应用,我院的这一成果将有望让中国在这一领域走在世界前列。

1. 研究发现:大气压低温等离子体诱导宫颈癌细胞凋亡
研究团队发现低温等离子体(NTP)暴露导致细胞内活性氧基团(ROS)的产生,继而抑制Bcl-2 的表达,增强Bax的表达,激活了线粒体介导的细胞凋亡。研究成果得到了时任国务院副总理刘延东的肯定与重要批示。
2. 研究发现:大气压低温等离子体诱导肺腺癌细胞凋亡
首次利用微阵列芯片技术,大规模系统分析了等离子体(NTP)处理所引发的复杂的基因表达谱变化情况,廓清了等离子处理对MAPK、TNF、P53等信号通路的调控。
3. 研究发现:大气压低温等离子体诱导肿瘤细胞发生焦亡
首次报导了等离子体(NTP)致死肿瘤细胞的新型死亡方式——焦亡。NTP通过激活ROS/JNK/Cytochrome C/Caspse-9/Caspse-3信号通路,进一步切割GSDME,导致肿瘤细胞发生焦亡型细胞死亡。
4. 自主研制:发展大气压低温等离子体技术,研制可移动等离子体治疗仪

